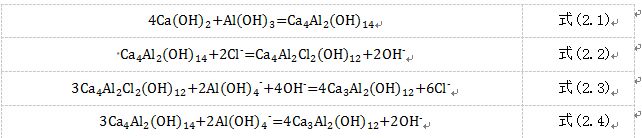| 化学沉淀法去除废水中氯离子的研究 | |||||||||||||||||||||||||||||||||||||||||||||||
| 作者: 发布于:2017/10/11 12:07:51 点击量: | |||||||||||||||||||||||||||||||||||||||||||||||
化学沉淀法去除废水中氯离子的研究 罗敏 (西安科技大学 地质与环境学院,陕西 西安 710600) 摘要:针对工业废水中存在高腐蚀性的氯离子,以及引起的环境污染等问题,采用化学沉淀法(超高石灰铝法),展开了沉淀试剂与氯离子反应生成溶解度极小的沉淀达到降低废水中氯离子浓度的研究。通过实验考察反应时间、搅拌速度等反应因子对氯离子去除的影响并得到最佳工艺参数。根据实验结果可以看出,超高该方法对于废水中的氯离子有理想的去除作用。在常温,投药比n(Ca):n(Al):n(Cl) 为6:2.4:1、搅拌时间为40min、搅拌速度为200r/min时,废水中氯离子的去除效果最理想能够达到58.82%,废水中氯离子的浓度由500mg/L降至205.88mg/L,低于标准(300mg/L),去除率达到工业要求的循环冷却水(GB/T 19923—2005)中Cl-质量浓度标准中的“敞开式循环冷却水系统补充用水标准”。超高石灰铝法操作简单,成本低廉,适合用于处理工业废水。 关键词:超高石灰铝法;氯离子;去除率;废水 自改革开放以来,我国的经济不断腾飞,工业化水平逐渐提高。近几年来,我国的数字经济以两位数的增长速度再创新高。我国在获得可观的经济利益、增加财政收入、提高人民收入水平的同时,付出了惨痛的资源环境代价。尤其是水资源,我国水资源污染事故发生频繁,水资源不仅是战略性的经济资源,也是保障人民生活品质的基准。干净并且达到水质标准的水源是开展各类工业活动的第一条件。近几年我国用水总量正逐渐靠近国务院确定的2020年年用水总量控制指标。当一个国家的用水量超越该国家水资源的20%,极引发水资源危机的可能性极大。我国的水资源的过度开发,相继造成水资源枯竭、过量开采的问题。水资源不足和需求不断扩大的矛盾也在逐渐加剧[2]。 由于生物法不能直接去除废水中的氯离子,大多数工业废水处理氯离子的目的仅仅为生物处理做前期准备,以及达到国家行业要求的循环冷却水中Cl-质量浓度标准。仅为去除废水中的氯离子而达标的做法相对较少,这也就造成了人们对氯离子危害没有足够的认识以及缺少对氯离子去除的重视[2,3]。国内外有利用热力法、电渗析法、反渗透法、沉淀法等,沉淀法最为经济便捷,针对含氯(500mg/L)废水研究其工艺参数对处理效果的影响。希望能找到最高效的方法去处理废水中的氯盐,达到水质标准,减轻对生态环境的危害。 1研究对象
某些工业废水中氯离子浓度较高,对工业设备腐蚀严重,影响正常生产,其中Cl-的浓度高达800mg/L-1000mg/L,更有甚者可达到3000mg/L[4]。含有高浓度Cl-的废水会造成很多环境问题,其中包括: (1)含氯废水排放到地表,会造成土壤盐渍化,抑制植物生长。 (2)Cl-含量过高时会对金属管道设备还有构筑物造成严重的腐蚀作用,阻碍了设备的正常运行和新工艺的实现,降低了产品的质量。 (3)含氯废水排放到水体中,会破坏水体中的水盐平衡,Cl-浓度较高时会造成水生生物的死亡。 (4)含氯废水还会污染到地下水,进而影响到饮用水,在人体饮用后对身体健康造成一定威胁。 2工艺选用
化学沉淀法是采用能与Cl-产生沉淀的金属离子如Ag+ 、Hg+、Ca2+和Al3+生成沉淀,在进行去除。该方法的操作简便,污染程度轻。该方法的关键是加入的处理试剂,在找廉价易得的沉淀剂方面有很大的发展前景[5-7]。 超高石灰铝法在去除废水中的氯离子方面能够达到满意的效果。该方法是利用氧化钙与偏铝酸钠作为沉淀试剂,投加到含氯废水中与Cl-反应生成不溶性的沉淀Ca4Al2Cl2(OH)12从而达到去除氯离子的目的。弗氏盐的首次发现是P. M. Friedel[8,9]在1897研究关于AlCl3的化学反应期间得到的,并以此命名。作为弗氏盐的一种, Ca4Al2Cl2(OH)12具有稳定的层状结构,是由Ca2Al(OH)6+和Cl-组成的层状化合物。 沉淀法不具有传统工艺的局限性,同时可以处理高浓度含氯废水,运行成本低,操作简单,耗能低,针对高氯废水对环境的危害大,对机械设备造成严重的腐蚀等问题,为获得满意的氯离子去除效果。本实验采用化学沉淀法作为处理含氯废水的处理工艺。樊响[10]为去除废水中的氯离子,采用超高石灰铝法,在石灰、偏铝酸钠以及初始Cl-摩尔浓度比例为5:2:1的条件下,去除废水中的Cl-获得较好的结果。公新忠[11]等采用石灰乳和偏铝酸钠去除含有F-和Cl-的酸性废水,在反应时间为5分钟且偏氯酸钠和氯离子的质量浓度比为1:10的条件下,废水中的Cl-去除率可以达到60%。Bikul[12]运动熟石灰和偏铝酸钠处理含有Cl-的废水,也获得较为理想的结果。考虑对环境的影响以及节约成本,本实验采用超高石灰铝法以CaO与NaAlO2作为沉淀试剂去除废水中的Cl-。通过实验考察反应时间、最佳配药比、搅拌速度等反应因子对氯离子去除的影响并得到最佳工艺参数。 3实验
3.1实验原理
采用超高石灰铝法,模拟含氯废水(500mg/L),向废水中投加一定量的氧化钙和偏铝酸与废水中氯离子反应生成沉淀物Ca4Al2Cl2(OH)12达到去除氯离子的目的。在反应过程中由于反应物以及反应条件的改变共会产生三种固体产物,Ca4Al2(OH)14 、Ca4Al2Cl2(OH)12 、Ca3Al2(OH)12。Ksp(Ca4Al2Cl2(OH)12)= 10-27.10,Ksp(Ca4Al2(OH)14)=10-25.02。因为Ksp(Ca4Al2Cl2(OH)12)
3.1.1实验药剂及仪器
在试验过程中,反应及水质分析所用到的实验试剂如下表3.1所示,所用到的实验仪器如下表3.2所示。
表3.1反应及水质分析所用试剂
表3.2反应及水质分析所用仪器
3.2实验方法
本实验采用氯化钠配置的溶液作为模拟含氯废水,称量0.8239g的NaCl溶解于1L的纯水中,向Cl-浓度为500mg/L的模拟废水中加入一定的氧化钙和偏铝酸钠,设置不同的搅拌速度和搅拌时间进行反应,反应后取上层清液进行过滤、稀释,根据 GB/T 15453—2008采用标准硝酸银溶液滴定氯离子,分析氯离子的质量浓度并计算出氯离子的去除率。 4结论及分析 4.1不同反应因子对氯离子去除率的影响
4.1.1不同n(Ca):n(Al)对氯离子去除率的影响
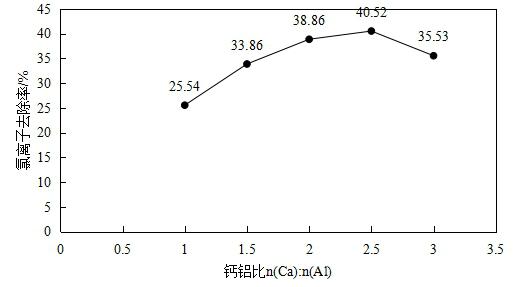
如图所示,随着n(Ca):n(Al)的逐渐增大,的变化趋势为先增大后减小。因为最初反应生成的Ca4Al2Cl2(OH) 12层状结构没有完全成型,Ca4Al2Cl2(OH) 12的层板间还能继续容纳Cl-; 随着Cl-不断进入结构使得层状结构容纳的Cl-达到最大化时,即钙铝比为2.5:1时,Cl-的去除率也达到了最大为40.52%,这时Ca4Al2Cl2(OH) 12的层状结构基本成型;当n(Ca):n(Al)大于2.5:1时,一部分的Ca4Al2Cl2(OH) 12的层状结构会发生改变,层板间所容纳的Cl-会减少,导致氯离子的去除率有所下降。该试验得出n(Ca):n(Al)的最优比为2.5:1。 4.1.2不同n(Ca):n(Cl)对氯离子去除率的影响
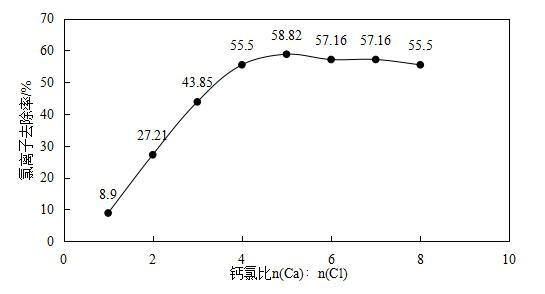
如图所示,随着n(Ca):n(Cl)的不断增加,氯离子的去除率呈现的趋势为先增大后减小。当n(Ca):n(Cl)小于6:1时,生成的Ca4Al2Cl2(OH) 12层状结构没有完全成型,Ca4Al2Cl2(OH) 12的层板间还能继续容纳更多的Cl-,所以氯离子去除率逐渐增加。随着Cl-不断进入结构使得层状结构容纳的Cl-达到最大化,氯离子去除率达到最大,n(Ca):n(Cl)等于6:1时Ca4Al2Cl2(OH) 12的层状结构基本成型。当n(Ca):n(Cl)大于6:1时一部分的Ca4Al2Cl2(OH) 12的层状结构会发生改变,层板间所容纳的Cl-会减少,导致氯离子去除率有所下降。本试验得出n(Ca):n(Cl) 最佳的值为6:1。分析得出n(Ca):n(Al):n(Cl)的最优比为6:2.4:1。 4.1.3不同的搅拌时间对氯离子去除率的影响
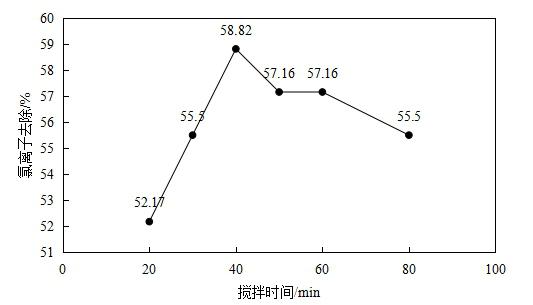
如图所示随着搅拌时间的逐渐增大,氯离子去除率呈现的变化趋势为先增大后减小。当搅拌时间小于40min时,主要生成不溶性的Ca4Al2Cl2(OH) 12,氯离子去除率逐渐增大并达到最大值;当搅拌时间大于40min时,由于溶液中的反应并不是单一的,在生成Ca4Al2Cl2(OH) 12的同时,部分的Ca4Al2Cl2(OH) 12转换为Ca3Al2(OH)12使得Cl-的去除率呈现出下降趋势并达到稳定状态。因此,分析得出最佳搅拌时间为40min。 4.1.5不同的搅拌速度对氯离子去除率的影响
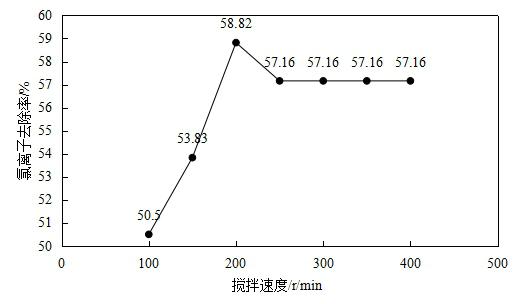
如图所示,随着搅拌速度的逐渐增加,氯离子去除率呈现的趋势为出先增加后减小最后进入平稳的状态。当搅拌速度小于200r/min时,生成的Ca4Al2Cl2(OH) 12层状结构没有完全成型,Ca4Al2Cl2(OH) 12的层板间还能继续容纳更多的Cl-,所以氯离子去除率逐渐增加,并随着Cl-的不断插入使得层状结构容纳的Cl-达到最大化时,氯离子的去除率也达到了最大值,这时层状结构成型。当搅拌速度大于200r/min时,Ca4Al2Cl2(OH) 12的层状结构被破坏,使得一部分的Ca4Al2Cl2(OH) 12转换为Ca3Al2( OH)12,氯离子的去除率也随之下降。因此,本实验分析得出最佳搅拌速度为200r/min。 4.2结论
本实验针对高氯废水对环境的危害大,对机械设备造成严重的腐蚀等问题,采用超高石灰铝法(化学沉淀法),展开了沉淀试剂与氯离子反应生成溶解度极小的沉淀达到降低废水中氯离子浓度的研究。通过实验考察反应时间、搅拌速度、n(Ca):n(Al):n(Cl)等反应因子对氯离子去除的影响。结论如下: (1)通过实验研究在反应前控制搅拌速度为200r/min,搅拌时间为40min,反应温度为常温,n(Ca):n(Al):n(Cl) 为6:2.4:1,的条件下,Cl-的去除效果最佳,Cl-的浓度由500mg/L降低至205.88mg/L低于标准(300mg/L),去除率达到工业要求的循环冷却水(GB/T 19923—2005)中Cl-质量浓度标准中的“敞开式循环冷却水系统补充用水标准”。 (2)当n(Ca):n(Al):n(Cl)超过6:2.4:1时,部分的沉淀物Ca4Al2Cl2(OH) 12转换为Ca3Al2(OH)12使得氯离子的去除率呈现出下降趋势。 (3)超高石灰铝法去除Cl-的反应速度较快,40min就能完成的去除反应并达到最佳的效果,由于该方法的化学反应并不单一,随着反应时间的延长,促使部分Ca4Al2Cl2(OH) 12转换为Ca3Al2(OH)12,降低了氯离子的去除率,不利于主反应的进行。 (4)随着搅拌速度的增加,增大了溶液中Cl-与处理剂的接触面积,促进了Ca4Al2Cl2(OH) 12结构的成型,Cl-的去除率也逐渐增大并达到平稳状态。 (5)本实验是采用纯水配置的模拟含氯废水,不含有其他的杂质离子。而实际处理的污水在进行去除氯离子的同时会受到杂质的干扰,实际处理废水的Cl-去除率与实验模拟得到的Cl-去除率会有一定的出入。 参考文献
[1] 秦天玲, 严登华, 宋新山, 等. 我国水资源管理及其关键问题初探[J]. 中国水利, 2011, (03): 11-15. [2] 武杰, 柴涛, 房亚玲. 高氯含量废水中氯离子的去除研究[J]. 现代化工,2016, (04): 101-103. [3] 张强, 肖世伟, 孙永华,等. 沉淀法去除废水中氯离子[J]. 化学工程师, 2015, (02): 20-22+29. [4] 程志磊, 杨保俊, 汤华伟, 等.超高石灰铝法去除水中氯离子实验研究[J]. 工业水处理, 2015, (05): 38-41. treatment, 2015, (05): 38-41. [5] 阮东辉,刘发强, 李长青, 等.超高石灰铝法脱除废水中高浓度氯离子的研究[J]. 石化技术与应用, 2016, (01): 29-31. [6] Mechanism of Friedel’s salt formation in cements rich in tri-calcium aluminate[J] . A.K. Suryavanshi,J.D. Scantlebury,S.B. Lyon. Cement and Concrete Research . 1996 (5) [7] 李永生, 郭慧. 工业水中氯离子测定方法的进展[J]. 工业水处理, 2007, (04): 1-5. [8] 安泰莹, 文庆珍, 朱金华. 氯离子测定方法研究进展[J]. 河南化工, 2013, (Z2): 8-11+24. [9] 郝志宁. 水中氯离子的测定方法及其研究进展[J]. 环境科学与管理, 2016, (05): 162-164. [10] 樊响. 超高石灰铝法去除循环冷却水中氯离子的试验研究[J]. 冶金设备, 2010, (S1): 36-38+144. [11] 公新忠, 丁德馨, 李广悦, 等. 含氟离子和氯离子酸性废水处理技术[J]. 环境工程学报, 2012, (09): 3157-3160. [12] Bikul’ chus G,Chlorride removal from reinforced concrete and relevant loss of strength[J] . Protection of Metal , 2005 , 41(5) : 520-522. 作者简介:罗敏(1994-),女,四川自贡人,西安科技大学地质与环境学院本科生,Email:876098550@qq.com (责任编辑:张仲民)
|